


BROTE HISTÓRICO La epidemia ya cuenta con más de 151 mil afectados y 106 muertos. Pese a que la vacuna fue avalada el año pasado por la ANMAT, aún existen algunas consideraciones ante su aplicación de forma masiva. Qué opinaron los expertos.

Argentina enfrenta el peor brote de dengue de su historia. Hasta el momento, según los últimos datos del Boletín Epidemiológico Nacional, se registraron más de 151 mil casos. Sin embargo, el dato más alarmante es que, en lo que va de la epidemia, se contabilizan 106 muertos, siendo que aún restan varias semanas para que finalice la temporada estacional de la patología. El año anterior, al totalizar las 52 semanas epidemiológicas, se contabilizaron un total de 65 fallecidos.
En tanto, la vacuna tetravalente contra el dengue del laboratorio japonés Takeda (TAK-003), conocida como Qdenga, fue aprobada a fines de abril en Argentina por la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT). Es por eso que, desde distintos espacios comenzaron a reclamar su aplicación para frenar el brote.
El pasado 7 de marzo, se sumaron al análisis la voces de los expertos que pertenecen a la Comisión Nacional de Inmunizaciones (CoNaIn) en una reunión extraordinaria en el marco del brote que se registra en todo el país. En el resumen del encuentro, que es de público acceso, recomendaron comenzar a delinear una estrategia de vacunación, al tiempo que aclararon las razones de por qué debía desarrollarse de forma selectiva y para determinados grupos etarios y poblacionales.

Según consta en la página 7 de documento, la CoNaIn considera:
Avanzar en la implementación de una estrategia focalizada de vacunación contra el dengue con vacuna Qdenga®.
Definir como criterio de selección la priorización de los departamentos según incidencia acumulada y el aporte total de casos.
Población objetivo: grupo de edad según análisis técnico.
Implementar un trabajo de modelaje prospectivo para la identificación de los departamentos a incluir en la estrategia.
Sin embargo, los expertos aclararon algunos puntos a tomar en cuenta. Pese a que se encuentran comprobados los datos de seguridad e inmunogenicidad para su aprobación mediante el ente regulador nacional, de acuerdo a lo expresado por el Grupo de trabajo de vacuna contra el dengue perteneciente a la CoNaIn, se debe analizar:
La ausencia de datos de eficacia clínica en personas mayores de 16 años. Al igual que como se ha hecho con otras vacunas, la eficacia en personas de mayor edad se interpreta en base a estudios de inmuno puente (previamente presentados a esta comisión). No se cuenta con un correlato clínico de protección demostrado.
La vacuna presenta datos de inmunogenicidad para los cuatro serotipos, en cuanto a la eficacia hay evidencia que en personas seropositivas la vacuna previene la infección contra los cuatro (4) serotipos y en personas seronegativas no mostró eficacia para prevenir la enfermedad sintomática causada por los serotipos DEN-3 y DEN-4 ni hospitalizaciones por DEN-3. No hubo casos suficientes en la muestra del estudio pivotal para demostrar eficacia contra DEN-4. No pudo verse protección contra DEN- 3 y DEN- 4 en personas seronegativas, ni a los 12 ni a los 54 meses de seguimiento post segunda dosis, en población de 4 a 16 años en zonas endémicas.
Seguridad en personas mayores de 60 años: no hay datos fehacientes, ANMAT analizó datos acerca de la seguridad en adultos mayores, que serán facilitados para contemplar en la evaluación que se está realizando. La vacuna en Argentina está aprobada sin límite de edad, también la EMA la aprobó con esta modalidad. Brasil, por otra parte solo la aprueba hasta los 60 años. Es fundamental ante la epidemia de dengue en nuestro país y el uso de la vacuna en privado, analizar datos de seguridad y de laboratorio, es decir, la necesidad de diferenciar si las pruebas PCR positivas en personas vacunadas con síntomas compatibles, se deben a la infección natural por el virus del dengue o a la viremia postvacunal (como se describe en el prospecto de la vacuna).
"En cuanto a recomendaciones de organismos internacionales, el Grupo Técnico Asesor en Vacunación de la Organización Mundial de la Salud (OMS - SAGE), menciona que se podría considerar la incorporación de la vacuna en escenarios de alta carga de enfermedad y alto índice de transmisión", afirman en la sección a la cual se hace referencia al Grupo de trabajo de vacuna contra el dengue perteneciente a la CoNaIn. Es por eso que enumeran:
En primer lugar, para maximizar el impacto en salud pública, ya que, en estos escenarios, la población de niños, niñas y adolescentes es la más afectada.
Segundo, para minimizar el riesgo de enfermedad potenciada por anticuerpos en personas seronegativas. Sugieren implementarla en personas de 6 a 16 años. Uno o dos años antes de la edad pico de hospitalizaciones por dengue.
Instrumentación de un estudio sólido de fase 4 para evaluar seguridad.
Además, señalaron que al estimar el "número necesario de personas a vacunar para evitar un evento de dengue virológicamente confirmado. Siempre que se considere un escenario de incidencia similar a la ocurrida durante el estudio pivotal de fase III de Takeda (TIDES), la de un país endémico, se necesitan vacunar 10.000 personas de 4 a 16 años con dos dosis para reducir alrededor de 5.000 eventos en cinco (5) años en ese grupo poblacional".
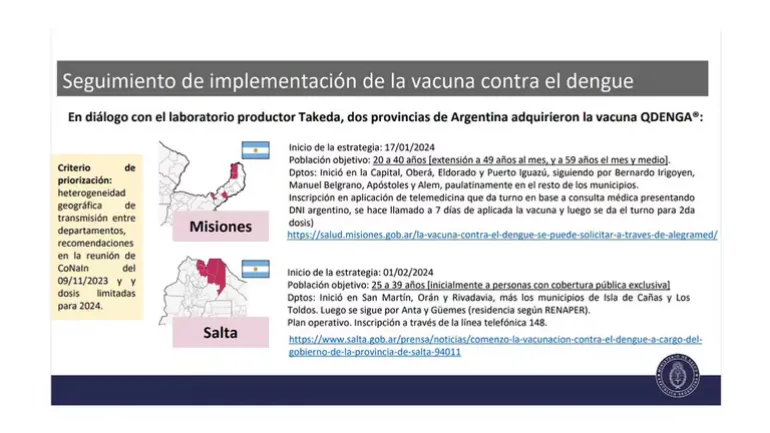
Vale recordar que Misiones, que comenzó con la estrategia de vacunación a mediados de enero, y Salta, que realizó lo propio el primer día de febrero, son las dos únicas provincias que establecieron una estrategia de inmunización y comenzaron con su aplicación a grupos poblacionales específicos. En ambas jurisdicciones, la presencia de la enfermedad logra, en algunas oportunidades, permanecer con casos incluso en invierno.
En Misiones, por tanto, "se estableció como población objetivo a personas de 20 a 40 años. Posteriormente fue ampliando el grupo objetivo, y actualmente se ha incluido la población entre 20 y 59 años", destacan los expertos de la CoNaIn. Al tiempo que advierten que en Salta se está "vacunando a personas de 25 a 39 años con cobertura pública exclusiva". "Ambas provincias gestionaron de manera directa con el laboratorio Takeda la adquisición de la vacuna", aclaró la doctora Verónica Lucconi Grisolía, de la Dirección de Control de Enfermedades Inmunoprevenibles (DiCEI).
Fueron parte de esta reunión extraordinaria: autoridades del Ministerio de Salud de la Nación, incluyendo al Dr. Andrés Scarsi (Secretario de Acceso y Equidad en Salud), al Dr. Hernán Seoane (Subsecretario de Planificación y Programación Sanitaria), al Dr. Federico Pedernera (Subsecretario de Vigilancia Epidemiológica, Información y Estadísticas de Salud), a la Dra. Florencia Bruggesser (Directora de Control de Enfermedades Inmunoprevenible), y al Dr. Mauro Bertolini (Director de Control de Enfermedades Transmitidas por Vectores).
Asimismo, participaron miembros del núcleo central, tales como la Dra. Angela Gentile, Dra. Ana Ceballos, Dra. Andrea Uboldi, Dra. Daniela Hozbor, Dra. Gabriela Barbas, Dr. Ricardo Ruttimann, Dr. Guillermo Docena y Dr. Ignacio Maglio. Los representantes de las regiones del Programa Ampliado de Inmunizaciones también estuvieron presentes, incluyendo a Lic. Fabio Muñoz (CUYO), Dra. Adriana Jure (NOA), Dra. Julio Arroyo Danar (NEA), Dra. Ana Bertone (SUR) y Erika Bartel (CENTRO).
De igual manera, asistieron representantes de sociedades científicas como la Sociedad Argentina de Infectología Pediátrica (SADIP) con la Dra. María Marta Contrini8, Sociedad Argentina de Pediatría (SAP) representada por Dra. Carlota Russ, Sociedad Argentina de Infectología (SADI) por Dra. Hebe Vazquez, Asociación Argentina de Microbiología (AAM) por Dra. Silvia González Ayala, Sociedad Argentina de Vacunología y Epidemiología (SAVE) con la Dra. Iris Aguilar, y la Sociedad Argentina de Enfermería (FAE) por Lic. Rubén Lastra, entre otros.